Tabel periodik adalah susunan unsur kimia berdasarkan kemiripan sifat di antara zat tersebut. Tabel ini terus diupdate berdasarkan hasil riset paling baru terkait keberadaan di alam dan perubahan sifatnya.
Saat ini terdapat 118 unsur dengan nomor atom 1 untuk unsur Hidrogen (H) dan 118 adalah Oganesson (Og). Tabel periodik bertujuan memudahkan siswa memahami berbagai unsur dan sifat-sifatnya di alam, termasuk kemungkinannya bereaksi dengan zat lain.
Pengertian Sistem Periodik
Tabel periodik disusun berdasarkan sistem periodik yang berlaku pada berbagai unsur di alam. Mengutip dari buku Seri IPA Kimia 1 SMP Kelas VII yang ditulis Crys Fajar Partana, M.Si., sistem periodik adalah metode pengelompokkan unsur berdasarkan sifatnya yang mirip.
SCROLL TO CONTINUE WITH CONTENT
Kata periodik mengacu pada pengulangan suatu karakter unsur pada interval tertentu. Sehingga, ada beberapa unsur dengan sifat yang serupa pada satu golongan. Sifat ini bisa berubah berdasarkan kondisi unsur tersebut di alam.
Kolom vertikal (dari atas ke bawah) menunjukkan golongan elemen dengan sifat yang saling mendekati (mirip). Sedangkan, deretan horizontal (periode) dalam tabel dibuat untuk unsur yang mengalami perubahan sifat secara periodik.
Golongan Unsur dan Periode Dalam Tabel Periodik
Tabel periodik tersusun atas sejumlah golongan unsur dan periode. Berikut rincian periode dan unsur dalam setiap golongan yang dirangkum dari Modul Kimia Dasar karya Dr. Yusnidar Yusuf. M. Si:
Periode dalam tabel periodik
Dalam sistem periodik modern, periode diletakkan pada kolom horizontal. Berdasarkan konfigurasi elektronnya, periode suatu unsur menunjukkan nomor kulit tertentu yang sudah terisi oleh elektron (n terbesar). Adapun 7 periode beserta unsurnya dalam sistem periodik modern adalah sebagai berikut:
- Periode 1 (Periode sangat pendek): H dan He.
- Periode 2 (periode pendek): Li, Be, B, C, N, O, F, dan Ne.
- Periode 3 (Periode pendek): Na, Mg, Al, Si, P, S, Cl, dan Ar.
- Periode 4 (Periode panjang): K, Ca, Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Ga, Ge, As, Sc, Br, dan Kr.
- Periode 5 (Periode panjang): Rb, Sr, Y, Zr, Nb, Mo, Tc, Ru, Rh, Pd, Ag, Cd, In, Sn, Sb, Te, I, dan Xe.
- Periode 6 (Periode sangat panjang): Cs, Ba, golongan lanthanida, Hf, Ta, W, Re, Os, Ir, Pt, Au, Hg, Tl, Pb, Bi, Po, At, Rn.
- Periode 7 (Periode sangat panjang): Fr, Ra, golongan aktanida, Rf, Db, Sg, Bh, Hs, Mt, Ds, Rg, Cn, Nh, Fl, Mc, Lv, Ts, Og.
Golongan dalam tabel periodik
Dalam tabel periodik yang dikeluarkan International Union of Pure and Applied Chemistry (IUPAC), unsur-unsur digolongkan menjadi:
- Bukan logam (nonmetal): gas mulia, reaktif nonmetal, halogen.
- Logam (metal): metaloid, usai transisi (post transition metal), transisi (transition metal), lantanida, aktanida, alkali tanah, dan alkali.
Tabel Periodik IUPAC
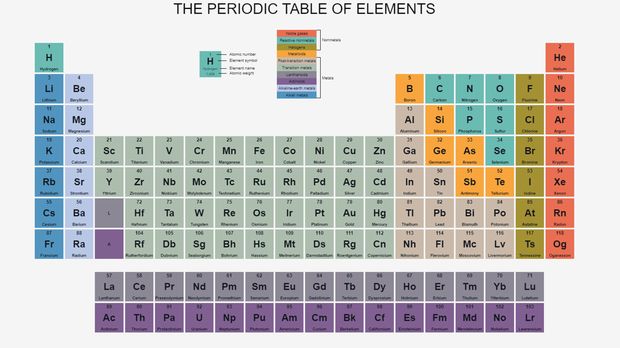 Tabel periodik 2024 yang diperbarui pada 2022. Foto: IUPAC Tabel periodik 2024 yang diperbarui pada 2022. Foto: IUPAC |
Penggolongan unsur dalam tabel periodik IUPAC berbeda dengan sebelumnya. Tabel periodik tak lagi menggunakan golongan utama (A) yang terdiri dari:
• Golongan 1A: H, K, Li, Na, Rb, Cs, dan Fr.
• Golongan 2A: Be, Mg, Ca, Sr, Ba, dan Ra.
• Golongan 3A: B, Al, Ga, In, Ti, dan Nh.
• Golongan 4A: C, Si, Ge, Sn, Pb, dan Fl.
• Golongan 5A: N, P, As, Sb, Bi, dan Mc.
• Golongan 6A: O, S, Se, Te, Po, dan Lv.
• Golongan 7A: F, Cl, Br, I, At, Ts.
• Golongan 8A: He, Ne, Ar, Kr, Xe, Rn, Og
Tabel periodik IUPAC masih menggunakan golongan transisi, namun tidak lagi memberi nama 1B-8B. Sebelumnya logam pada golongan transisi terdiri dari:
• Golongan 1B: Cu, Ag, Au, dan Rg.
• Golongan 2B: Zn, Cd, Hg, dan Cn.
• Golongan 3B: Sc, Y, golongan lantanida, dan aktanida.
• Golongan 4B: Ti, Zr, Hf, dan Rf.
• Golongan 5B: V, Nb, Ta, dan Db.
• Golongan 6B: Cr, Mo, W, dan Sg.
• Golongan 7B: Mn, Tc, Re, dan Bh.
• Golongan 8B: Fe, Ru, Os, Hs, Co, Rh, Ir, Mt, Ni, Pd, Pt, dan Ds.
Cara Membaca Tabel Periodik
Hal paling mendasar yang harus dipahami untuk menghafal unsur dalam tabel periodik adalah mengetahui cara membacanya. Tabel periodik dibaca mulai dari kiri atas sampai ke kanan bawah.
Unsur kimia yang terletak di bagian kiri atas hingga bawah menandakan bahwa unsur-unsur tersebut memiliki nomor atom terkecil. Sedangkan unsur yang terdapat di bagian kanan hingga bawah merupakan unsur dengan nomor atom lebih besar.
Sebagai catatan, nomor atom merupakan jumlah proton dalam inti atom suatu unsur. Nomor atom paling kecil adalah 1 milik unsur H, sedangkan terbesar adalah Og dengan 118. Tabel periodik terus diperbarui berdasarkan riset, pastikan detikers mengetahui hasil studi terbaru.
(row/row)


























































