Tabel periodik merupakan tabel berisi susunan unsur-unsur kimia yang dipelajari ketika masuk ke bangku SMA. Tabel periodik mungkin terlihat rumit secara sekilas. Namun, tabel periodik sebenarnya justru mempermudah kita untuk mempelajari unsur-unsur kimia yang jumlahnya sangat banyak
Unsur-unsur kimia yang ada pada tabel periodik jumlahnya sangat banyak dengan sifat yang berbeda-beda. Tabel periodik dibuat dengan tujuan untuk mempermudah mengenal nama unsur melalui pengelompokan yang ada.
Agar kamu bisa lebih memahami tabel periodik, simak pengertian dan cara membacanya berikut ini.
SCROLL TO CONTINUE WITH CONTENT
Pengertian Tabel Periodik
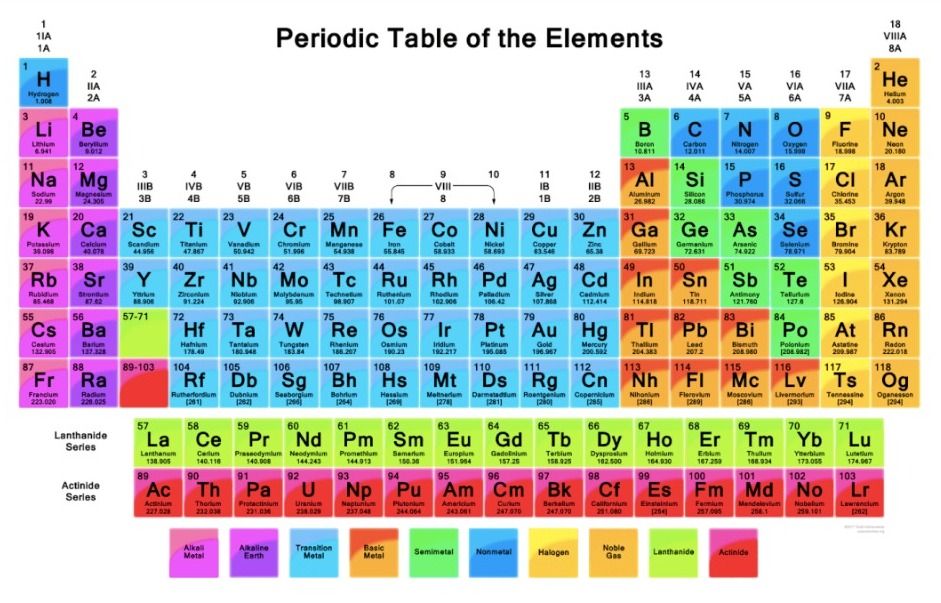 Gambar Tabel Periodik Unsur Kimia. Foto: dok. modul belajar Kemdikbud Gambar Tabel Periodik Unsur Kimia. Foto: dok. modul belajar Kemdikbud |
Tabel periodik merupakan unsur-unsur kimia yang disusun dalam bentuk tabel. Susunan unsur-unsur kimia ini berdasarkan pada nomor-nomor atom yang dimilikinya.
Nomor atom yang tersusun itu berdasarkan jumlah proton dalam konfigurasi elektron tertentu dengan kesamaan sifat yang dimiliki unsur kimia.
Tabel periodik terbagi atas empat blok, yaitu blok s, p, d, dan f. Dalam satu baris atau satu periode, bagian kiri menunjukkan sifat logam dan bagian kanan menunjukkan sifat non logam.
Istilah-istilah dalam Tabel Periodik
Agar bisa memahami tabel periodik, ada sejumlah istilah yang perlu kamu ketahui. Simak istilah-istilah dalam tabel periodik berikut ini.
1. Periode
Periode merupakan sebutan bagi baris horizontal yang ada pada tabel periodik. Tabel periodik memiliki 7 periode berdasarkan tingkat energi atom yang dimiliki.
Perlu diketahui bahwa tidak semua periode memiliki jumlah unsur yang sama. Periode 1 memiliki jumlah unsur terkecil, yaitu 2. Sedangkan jumlah unsur terbesar ada pada periode dengan 32 unsur.
2. Golongan
Jika periode merupakan baris horizontal, maka golongan adalah kolom vertikal pada tabel periodik kimia. Dalam mengklasifikasikan unsur, golongan memiliki peran yang sangat penting.
Golongan mencakup unsur-unsur dengan susunan elektron terluar yang sama. Unsur-unsur tersebut memiliki sifat kimia yang sama karena jumlah elektron terluarnya sama. Golongan ditulis dengan urutan bilangan romawi.
3. Blok S
Pada tabel periodik kimia, blok s merupakan unsur dari dua golongan, yaitu logam alkali dan alkali tanah. Blok s juga mencakup unsur tambahan, yaitu hidrogen dan helium.
4. Blok P
Pada tabel periodik kimia, blok p merupakan unsur-unsur dari enam golongan. Golongan unsur pada blok p antara lain golongan 3A hingga 8A. S
5. Blok D
Blok d pada tabel periodik terdiri atas 3 hingga 12 golongan mulai dari golongan 3B hingga 2B. Semua unsur kimia pada blok d merupakan logam transisi.
6. Blok F
Pada tabel periodik, unsur-unsur kimia yang tergabung di dalam blok f cenderung diletakkan di bagian bawah. Blok f tidak memiliki nomor golongan dan merupakan unsur lantanida dan aktinida.
Cara Membaca Tabel Periodik
Cara membaca tabel periodik tidak begitu sulit jika sudah mempelajari dan terbiasa. Membaca tabel periodik diawali dari bagian kiri atas hingga ke kanan bawah.
Unsur kimia pada bagian kiri atas hingga kiri bawah tabel periodik memiliki nomor atom terkecil. Sedangkan unsur kimia pada bagian kanan hingga ke bawah, memiliki nomor atom yang lebih besar.
Nomor atom yang dimaksud merupakan jumlah dari proton yang dimiliki oleh unsur-unsur kimia. Dalam tabel periodik, nomor atom dimulai dengan angka 1 hingga 118.
Itulah pengertian tabel periodik, istilah, dan cara membacanya yang bisa kamu pelajari. Semoga mudah dipahami ya, detikers!
(inf/inf)

























































